感染3要因① 病原体の観点から
日本を代表するウイルス、感染症の研究者として、人獣共通感染症(ズーノーシス)のリスク解析研究を牽引してこられた森川 茂先生※にお話を伺いました。
このインタビューは、2021年5月に当社研究フェロー村越が行いました。
※先生のプロフィールはページ下部にてご紹介しております。
村越:本日の話題の中心、新型コロナウイルス感染症COVID-19も、新興ウイルス感染症で、ズーノーシス※1に該当するわけですが、ズーノーシスの概念や考え方、定義を教えてください。
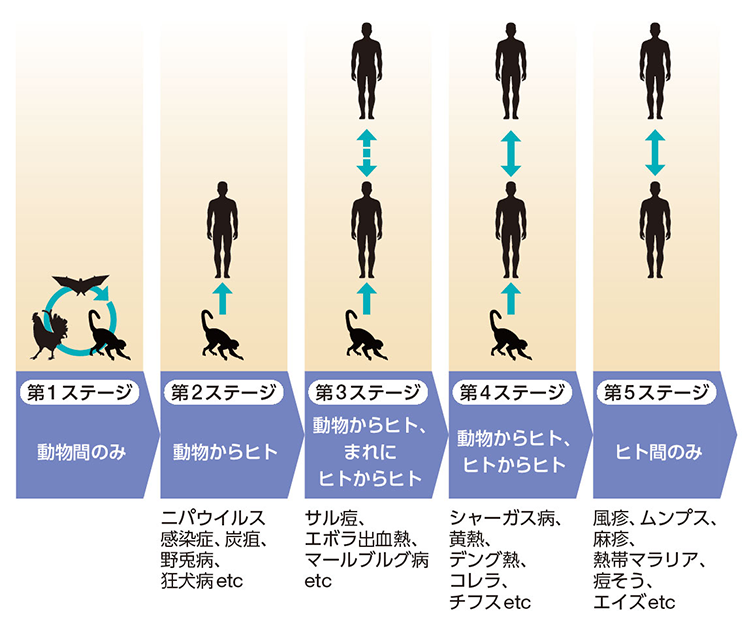
森川先生:ギリシャ語の「ズー(zoon)(動物)」と「オセス(nosos)(病気)」でズーノーシス、日本語では人獣共通感染症あるいは動物由来感染症といいます。ヒトと動物はいろいろな形で相互作用しながら生きているので、病原体が動物からヒトへ、ヒトから動物へ、あるいは動物から動物へ種を超えて感染することがあるのです。1970年ごろから次々と現れている新興感染症は、ほとんどがズーノーシスです。動物由来の病原体がヒトに感染するようになるまでには、5段階のステージを経るといわれています(図1)。第1ステージは、動物同士の感染で、ヒトへの感染性はありません。第2ステージに移行すると、動物からヒトへ感染するようになり、第3ステージでは、動物からヒト、さらに、まれにヒトからヒトへも感染するようになります。第4ステージに移行すると、動物からヒトへと感染し、ヒトからヒトへの感染も頻繁に起こるようになります。第5ステージに達すると、動物からの感染がなくなり、ヒト間での感染のみで感染するようになります。麻疹(はしか)やおたふく風邪、風疹などは第5ステージです。今はこれらの感染症を誰もズーノーシスとはいいませんが、もとは動物から来た感染症です。
我々が知らなかった新しい動物由来のウイルス感染症が発生した場合、多くは第2ステージ、つまりヒト間で感染しない内に収束します。ただ、第2~3ステージの感染症は、致死率が非常に高いことが多いです。致死率の高い感染症は、普通は第5ステージまでは移行しません。
村越:なぜ、致死率の高いものは第5ステージに移行しないのですか?
森川先生:致死率が高い感染症は、患者を隔離して、ヒト間の感染を遮断できるため、第5ステージには至らないというのが我々の見解です。また、血液や体液を介した感染はパンデミックにはなりにくい。パンデミックを起こすのはインフルエンザや今回のCOVID-19のように、ほぼ呼吸器への感染症です。
村越:2002年~2003年にかけて流行したSARSや2012年頃から出てきた MERSもCOVID-19に非常に似たコロナウイルスによる呼吸器感染症候群ですが、大きなパンデミックに至らなかったのはどんな理由からですか。
森川先生:キクガシラコウモリが起源といわれているSARSはCOVID-19よりも重症化率・致死率とも高いのですが、発症前の段階でヒトからヒトに感染することはほとんどなく、発症して入院した患者からの院内感染が主でしたので、病院内で抑え込むことができました。コウモリからのウイルスが伝播したラクダが感染源といわれているMERSも、重症化率・致死率ともに高いですが、上気道よりさらに深い肺の奥でウイルスが増えて症状を起こすため、咳や呼気に含まれるウイルスは多くなく、ヒトからヒトへはあまり感染しませんでした。ところがCOVID-19は、無症状の人が多く、さらに発症前でも感染するため、ここまで拡大してしまったわけです。
村越:感染に気付かないうちに、市中感染が起きていることが、感染拡大の要因なのですね。SARSコロナウイルス2型(SARS-CoV-2)のように、新しいウイルスというのは、毎年でてきているのでしょうか。
森川先生:高病原性鳥インフルエンザという言葉を聞いたことがあると思いますが、このウイルスは毎年出ています。発生すると、養鶏場の鶏を全処分することが法律で決められていますが、それは、ヒトに感染した場合に致死率が50%くらいになるため、ヒト-ヒト感染するようになったら大変だからです。日本ではまだヒトに感染した例はありませんが、海外では毎年ヒトに感染して死者が出ています。
村越:新しい感染症がどんどん出てくる背景にはどのようなことがあるのでしょうか。
森川先生:現在ヒトに感染して病気を起こすと知られているウイルスは、約1,000種類ですが、鳥類や哺乳類に感染する未知のウイルスが167万種ぐらいあると推測されていて、その内の60万~80万種のウイルスがヒトに感染する可能性を持つのではないかと推測されています※2。我々が知っているウイルスは、1%にも満たないということです。海の方を見ると、もっと無尽蔵にいるのではないかと言われています。
村越:いまある感染症は氷山の一角にすぎないということですね。
森川先生:未知のウイルスそれぞれが変異を起こしたり、ほかの動物を介してヒトに感染できるように変異したウイルスというのは、無尽蔵にあるでしょう。こうしたウイルスが原因の感染症で、パンデミックに至らず、よくわからない内に収束している例が、実はかなりあるのではないかと思います。
COVID-19の原因ウイルスであるSARS-CoV-2のゲノム配列は、キクガシラコウモリの仲間が持つウイルスに近いといわれていますが、ヒトに感染するためのスパイク部分の配列は、センザンコウから見つかったコロナウイルスの配列とそっくりです。コロナウイルスは遺伝子組み換えを非常に起こしやすいので、コウモリとセンザンコウが持つコロナウイルスが組み換えを起こし、ヒトに感染するようになったのではないかという説がSARS-CoV-2の起源として一番有力視されています。
ウイルス感染症は、ヒト-ヒト感染が広がっていく内に、ほかの動物にも感染してさらに変異を起こし、より病気を起こしやすいウイルスが生まれるというリスクもあるので、こうした部分の研究も急を要しますね。一度広まってしまうと、コントロールはますます難しくなるのです。少なくとも、私たちにとって身近なイヌ・ネコが病気を起こしてまたヒトに戻ってくるというようなウイルスが広がらないようサーベイランス※3をしたいと思っています。
村越:先生が提唱されているワンヘルス※4も、こうした感染症を医師と獣医師とが、協働して防ごうという考え方ですね。
森川先生:はい。ヒトも動物も環境も同じように健康であることが大切という考え方です。最近は、農業もワンヘルスの一部として考えられるようになりました。アジアでは、農薬や肥料に抗生剤を混ぜることが多く、それによって薬剤耐性菌が環境中に生まれてきます。この薬剤耐性菌がヒトや動物に感染すると、過去に抗生剤を使った治療をしたことがないのに、抗生剤が効かず治療が難しくなるというリスクがあります。ワンヘルスは、ヒト・動物を超えて環境も含めた広い視野で対応していくことが必要です。
村越:病気の人がたくさん出てきて初めてウイルスの関与がわかった最近の例というのは、ほかにどういうものがありますか?
森川先生:原因不明の致死率が高い病気が中国で次々発生したことで特定されたのが、ブニヤウイルスによるSFTS※5です。ウイルスをもったダニがヒトや動物を吸血することで発症します。農作物を荒らしにきたシカやイノシシが、ヒトの生活圏にダニを運び、ヒトやイヌ、ネコなどがダニに吸血されて、よりヒトに近い場所でウイルスが循環するようになったのです。日本では、2013年1月に初めて報告されて以来、西日本を中心に毎年感染者が出ていて、これまでに70人以上が亡くなっています。
以前、新興感染症の多くはアフリカで発生していましたが、最近中国やアジアでも増えているのは、野生動物との接点が増えたことに因ると思います。こうした地域では、生きた野生動物がマーケットで売られていますが、これも非常にリスクが高い。野生動物との接点を密にしないことは重要です。
村越:アジア圏特有の気を付けるべき感染症はありますか?
森川先生:狂犬病です。日本では今は撲滅されたのであまり関心がありませんが、発症すると致死率がほぼ100%の感染症です。アジアとアフリカで多く、一番はインドですが、今も世界中で年間5万人ほど発症しています。殆どが狂犬病にかかったイヌに噛まれたことが原因です。
村越:なるほど。野生動物だけではなく、身近な動物へも注意が必要ですね。
COVID-19は、発生からわずか1年ほどでワクチン接種が始まって、感染が広まり始めた当初はこれほど短期間にワクチンが開発されるとは想像もできなかった事ですが、他にも、感染症やコロナウイルスに関連した研究が日々ものすごい勢いで進んでいると感じます。
森川先生:やはりmRNAワクチンは画期的ですね。mRNAワクチン開発の難しさは、mRNAがヒトの免疫システムによって敵とみなされ、分解されたり翻訳が阻害されたりしてしまうことです。修飾ウリジンを応用していち早く、この課題を克服したのが、ファイザー社とモデルナ社です。mRNAは、体内で分解されて遺伝子変異を起こすリスクがないこともメリットです。ファイザー社、モデルナ社製のmRNAワクチン、アストラゼネカ社製のアデノウイルスベクターワクチン、これらは、2回接種することで、変異株に対しても発症や重症化を防ぐ効果があるという報告が、イギリスの政府研究機関PHE(Public Health England)はじめ、様々な研究機関から発表されています。また、治療薬に関しても研究が進んでいます。SARSが現れた20年前に比べ、科学技術のレベルが格段に進歩していることも見逃せません。また、各国が予算を大量に投入していることも研究を加速させています。
村越:次々と変異株が現れて、コロナ収束の兆しが見えない中ですが、ウイルスに打ち勝とうと世界中で研究が進んでいることは朗報ですね。
では最後にメッセージをお願いします。
森川先生:COVID-19のように大規模なパンデミックを起こす感染症や、SFTSのように小規模ながら致死率の高い感染症は、これからも現れると思います。原因がわからない病気があったときには、ウイルスによる感染症を疑っていただきたいと思います。新しいウイルスが見つかり、その研究を感染拡大した時の備えにすることができます。疑いがあれば是非国立感染症研究所などに情報提供をお願いします。
村越:そういった情報提供も大変重要ですね。たくさんの貴重なお話をお聞かせいただき、誠にありがとうございました。
※1ズーノーシス:WHOによって、「ヒトと脊椎動物の間を自然の条件下で伝播する微生物による疾病及び感染症」と定義づけられる。
※2Dennis Carroll et al.(2018). The Global Virome Project. Science, 359, 872-874
※3サーベイランス:感染症の発生状況の調査・分析により、適切な感染対策を立案し、感染症のまん延と予防に役立てるシステム。
※4ワンヘルス(一つの健康):ヒトの健康を守るため動物や環境にも目を配って取り組もうという考え方。近年は、畜産業をはじめ幅広い分野で用いられている抗菌薬から薬剤耐性菌が発生し、それがヒトの感染症の原因となることが問題視されている。
※5重症熱性血小板減少症候群(SFTS):ダニ媒介感染症。発熱、嘔気、嘔吐、腹痛、下痢、下血、ときに、筋肉痛、神経症状、リンパ節腫脹、出血症状などを伴う。致死率は10~30%程度。2021年、初めて静岡県、千葉県で感染が確認された。予防策として、野外活動の際は、マダニに咬まれないよう、長袖・長ズボン、足を完全に覆う靴、帽子、手袋を着用し、首にタオルを巻くなど肌の露出を少なくすることが大事。マダニを目視で確認しやすい明るい色の服を着用するとなお良い。
岡山理科大学獣医学部微生物学 教授
森川 茂先生

1981年東京大学農学部畜産獣医学科卒業、1983年同大学農学系大学院修士、獣医師、1991年同大学博士(農学)。
国立予防衛生研究所、英国オックスフォードNERCウイルス環境微生物学研究所、国立感染症研究所獣医科学部長を経て、2019年より現職。主に、人獣共通感染症のリスクや病原性、ワクチン開発などの研究に従事。2005~2011年WHO天然痘研究評価委員会委員、2007~2019年岐阜大学大学院客員教授、2008~2019年東京大学大学院農学生命科学研究科連携教授等を兼任。日本ウイルス学会監事、日本バイオセーフティ学会理事、日本獣医学会評議委員。